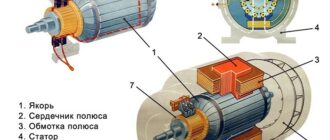
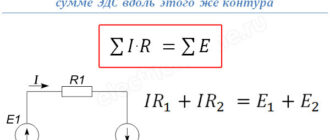Есть огромное количество методов выполнить самодельные батарейки. К огорчению, большая часть самодельных аккумов или никчемны, или потенциально небезопасны и сложны в изготовлении. Батареи из лимона и картофеля, обычно, очень слабенькие и требуют в качестве материала скоропортящегося органического растительного материала, в конструкцию свинцово-кислотных аккумов входят высокотоксичные и едкие химикаты и т.д.
Эта батарея изготовлена из очень обычных и доступных материалов, и обладает достаточной мощностью для работы устройств. Когда классические батареи недосягаемы эта батарея будет хорошим аварийным источником электроэнергии. Не считая того, ее можно просто перезарядить фактически от любого источника неизменного тока, она очень легкая и, в отличие от более распространенных алюминиево-воздушных батарей, не просит воздушного потока для работы.
Инструменты и материалы: -Алюминиевая фольга; -Соль (хлорид калия, кальция либо натрия будет работать, а бикарбонаты, карбонаты и гидроксиды — нет); -Источник слабоактивного металла (консервные банки либо медная проволока / трубки — хороший вариант); -Бумага (писчая бумага, бумажное полотенце либо туалетная бумага; -Клей ПВА; -Вода; -ПВХ-труба; -Клеевой пистолет; -Мультиметр; Шаг 1-ый: дизайн и теория Механизм работы батарей основан на хим реакции, известной как окислительно-восстановительная реакция. В окислительно-восстановительной реакции одно вещество окисляется (теряет электрон), а другое восстанавливается (приобретает электрон). Достаточно легко. Неважно какая батарейка устроена похожим образом, в ней неотклонимы три элемента, между которыми происходит хим реакция, в итоге которой появляется электричество: электроды — анод, катод, и электролит.
В этой алюминиево-металлической батарее две половины батареи пропитаны физиологическим веществом и разбиты специальной мембраной, пропускающей только ионы натрия и хлора. Алюминий с одной стороны начинает окисляться, в то же время как медь либо сталь на обратной стороне пробуют остаться размеренными.
В принципе неважно какая батарейка либо аккумулятор это две железные пластинки, помещенные в особое хим вещество – электролит. Одна пластинка подключается к плюсу, 2-ая к минусу. Пока батарею не трогают, на ней остается размеренное напряжение, к примеру, 3 либо 9 В. Стоит подключить к батарейке нагрузку, лампочку, вентилятор, как от плюса к минусу потечет ток. Напряжение начнет падать и сразу начнется окислительно-восстановительная реакция. Электроны начнут перетекать с отрицательной (-) пластинки назад на положительную, поддерживая тем разность потенциалов между ними.
Читайте также: Ленточный сборочный поток технические свойства – Ленточный сборочный поток | Механизм работы, устройство и установка, систематизация и технические свойства – на промышленном портале Myfta.Ru
Реакции бывают обратимыми (аккумулятор) и необратимыми (батарейка). Т.е. в батарейке реакция необратимая и ее нельзя зарядить, а в аккуме обратимая и он заряжается. Если подключить аккумулятор к зарядному устройству, ток снутри него начинает течь в оборотном направлении, другими словами – от «+» к «-». И реакция в электролите также начинает идти в оборотном направлении. В итоге, продукт реакции разлагается на начальные вещества. Аккумулятор «заряжается»
Естественно, этот процесс не нескончаем и наступит момент, когда одна из пластинок разрушится и хим реакция больше не сумеет перейти.
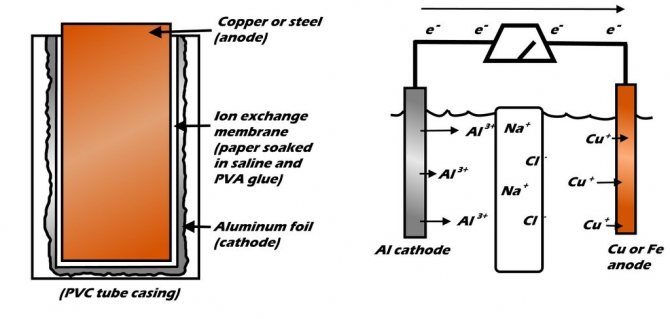
Шаг 2-ой: анод Анод должен быть изготовлен из металла, который наименее электроотрицателен, чем алюминий. Медь, сталь являются неплохими выбором, хотя медь работает идеальнее всего. Если применять наименее химически активный металл свинец либо серебро, то они не будут работать так же отлично. Мастер использовал маленькую медную трубу, которую скрутил в цилиндр. Так как это батарея размера D, он обрезал анодный до высоты обыденного D-элемента. Поперечник был незначительно меньше внутреннего поперечника секции трубы из ПВХ из которой будет изготовлен корпус элемента.

Шаг 2-ой: мембрана Дабы выполнить ионообменную мембрану, необходимо обернуть только-только изготовленный анод бумагой либо другим узким абсорбирующим материалом. Потом опустить конструкцию в соленую воду. Заместо обыкновенной соли можно применять к примеру, хлорид калия, нитрат либо сульфат щелочного металла. Соли кальция и магния не будут работать, так как соединения меди и железа с этими ионами в реакцию не вступают. После замачивания необходимо нанести на всю бумажную часть клей ПВА. Это предупредит проникновение большей части растворимых солей меди / железа на катодную сторону батареи. Далее необходимо дать клею высохнуть и опять пропитать в растворе соли. Более резвый метод отверждения клея, заключается в погружении покрытой клеем мембраны в раствор тетрабората натрия (бура), который практически немедля полимеризует клей ПВА и помогает прирастить его ионную проводимость.


Шаг 3-ий: катод Очередной принципиальной частью этой батареи является дюралевый катод. Это самый обычный шаг, необходимо просто оберните мембрану дюралевой фольгой. Удостоверьтесь, что дюралевая фольга не соприкасается с медным либо железным анодом.

Шаг 4-ый: корпус Сейчас необходимо отрезать пластиковую трубу и поместить вовнутрь батарею. С торцов батарея фиксируется термоклеем. Вполне закрывать батарею ненужно так как снутри будут перейти хим процессы и будет создаваться маленькое количество газа.

Шаг 5-ый: зарядка и проверка Аккумуляторная батарея готова, но ее необходимо зарядить. Можно применять фактически хоть какой источник неизменного тока, если ток не очень велик (до 5 А). Дабы зарядить аккумулятор, необходимо подключите анод к плюсу зарядного устройства, а катод к минусу. Во время зарядки ток начнет уменьшатся по мере того, как батарея набирает заряд. Это является неплохим признаком, и гласит о том, что батарея работает верно. После зарядки необходимо проверить аккумулятор мультиметром. Используя медный анод, мастер получил наибольшее напряжение 1,44 В после умеренного цикла зарядки. Наибольший ток, который он получил от батареи, был огромным для таковой самодельной батареи — 1.2 А. Для сопоставления, лимоновые либо картофельные батареи обычно выдают в наилучшем случае всего несколько миллиампер. Коммерческая батарея D-cell может выдавать ток более 5А.
Так же мастер провел тест, в каком сравнил свою батарею с реальным D-элементом на 1,5 В. Обе батареи тестировались с маленьким движком неизменного тока. При всем этом измерялся ток и скорость вращения мотора. И самодельная и промышленная батареи проявили приблизительно однообразные результаты.
Естественно, этот аккумулятор не безупречен. Ионообменная мембрана как и раньше пропускает некоторые растворимые соли меди на катодную сторону батареи, где они вступают в реакцию с образованием железной меди и нерастворимых оксидов и гидроксидов меди. Не считая того, дюралевый катод равномерно идёт в негодность, на самом деле, растворяется. Но, невзирая на это, батарея очень комфортна и может быть просто собрана и применена людьми в экстремальной ситуации. Увеличивая размер батареи, и подключая несколько ячеек последовательно либо параллельно, можно создавать либо хранить очень огромное количество энергии с маленькими затратами.

Источник (Source)
Становитесь создателем веб-сайта, публикуйте собственные статьи, описания самоделок с оплатой за текст. Подробнее тут.










Опасность перезаряда литиевых частей
С литиевыми элементами следует обращаться осторожно, так как в них сосредоточена большая энергия на малую площадь при полном заряде. Потому уже издавна в продаже имеются защищенные Li-ion и Li-pol батарейки.
Ещё в 1991 году компания Sony направила внимание на взрывоопасность Li-ion частей. В текущее время все без исключения батареи наматываются с двухслойным сепаратором между пластинами, дабы исключить риск внутреннего недлинного замыкания. Все фирменные батарейки снабжены платой защиты на полевом транзисторе, которая отключает их в следующих случаях:
- Аккумулятор чрезвычайно разряжен — ниже 2,5 В.
- Перезаряжен — выше 4,2 В.
- Подан очень большой ток заряда — более 1С (С является ёмкостью аккума в Ач).
- Куцее замыкание.
- Превышен ток нагрузки — более 5С.
- Некорректная полярность при заряде.

Для дополнительной подстраховки служит термопредохранитель, размыкающий цепь при перегреве литиевого элемента выше 90 °C.
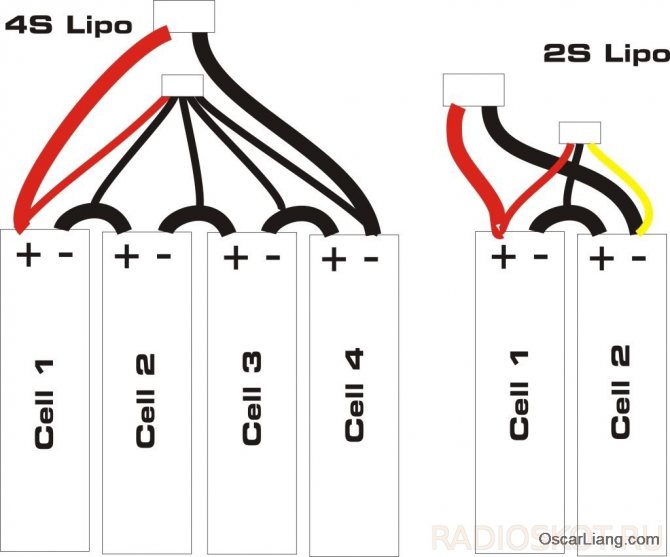
Как соединить литиевые батарейки?
Для сборки аккума из литиевых батареек можно использовать:
Читайте также: Как воткнуть пружину на триммер на заводилку
- пайку;
- соединительные коробки;
- неодимовые магниты;
- точечную сварку.
Пайку при заводской сборке используют очень изредка, так как литиевый элемент разрушается от нагрева, теряя при всем этом часть собственной ёмкости. С другой стороны, в домашних критериях пайка будет хорошим методом соединения батареек, так как даже маленькое сопротивление на контактах существенно понизит суммарное напряжение на общих клеммах. Воспользоваться необходимо массивным паяльничком на 100 Вт, и дотрагиваться им к литиевым батареям менее чем на две секунды.

Массивные редкоземельные магниты покрываются слоем никеля либо цинка, потому их поверхность не окисляется. Эти магниты обеспечивают красивый контакт между батарейками. Если возжелаете припаять проводок к магниту, не запамятовывайте о температуре Кюри, выше которой хоть какой магнит становится камушком. Приблизительно допустимая температура для магнитов составляет 300°С.
Если воспользоваться коробком для соединения аккумов, то становиться естественным большой плюс, так как так легче будет подобрать батарейки по напряжению либо поменять испорченный элемент.
Точечная сварка — лучший метод соединения литиевых частей, применяемый при сборке батарей для ноутбуков.
Брать готовый литиевый аккумулятор для машины либо байка нерентабельно, когда его можно собрать самому за более малую стоимость. Можно сберечь до 70 баксов, если не брать новейшую батарею ноутбука, а без помощи других поменять в ней элементы.
Об экономии при сборке массивных литиевых батарей для питания электроавтомобилей либо систем автономного электроснабжения дома судить тяжело, так как в этих случаях находятся дополнительные издержки на оборудование управления и контроля.
Как выполнить батарейку в домашних критериях
Привет все читателям «ИзобретайКи«! На просторах Ютуба нам попался увлекательный канал мастера на все руки Александра Полуняха, который просто делает батарейку в домашних критериях. Батарейки делаются из дюралевых банок от шипучих напитков, графитовых стержней, соленой воды и угольной крошки. Их мощности хватает на то, дабы зажегся светодиод либо малая лампочка.
Материалы для производства самодельной батарейки

Материалы для производства батарейки в домашних критериях
Дабы выполнить две батарейки для вас будет нужно следующее:
- Две дюралевые банки емкостью 500 мл.
- Два графитовых стержня.
- Угольная крошка либо пыль (подойдет маленькая угольная крошка, оставшаяся от костра).
- Кусок пенопласта шириной до 1 см.
- Парафиновые свечки.
- Соль и один литр воды.
- Светодиодная лампочка либо тестер для определения напряжения, которое выдает батарейка.
- Несколько проводков для подключения самодельных батареек к светодиодной лампочки.
- Острый ножик, которым можно резать узкий алюминий.
- Пластмассовая бутылка для производства воронки.
- Консервная банка и плоскогубцы
Мастерим батарейку в домашних критериях
- Ножиком вырежьте высшую часть банки.
Вырежьте высшую часть банки

Установите на дно банок пенопластовые круги

Воткните в банки графитовые стержни

Изготовьте из пластмассовой бутылки воронку
засыпьте вовнутрь банки угольную крошку,

Засыпьте в банки размельченную угольную крошку

Приготовьте солевой раствор
и залейте его в банку.

Залейте в банки солевой раствор

Залейте высшую часть банок расплавленным воском

Подсоедините провода к батарейкам

Итог — батарейки питают светодиод
Для наилучшего осознания процесса производства батарейки, предлагаем поглядеть видео «Как выполнить батарейку в домашних критериях».